【转自中国科学院微生物所】核苷(酸)类似物由于其作用靶点多为DNA聚合酶或RNA逆转录酶,能够干扰肿瘤和病毒细胞的核苷代谢,已应用于核苷类抗病毒药物和抗癌药物,使得医药行业对核苷(酸)发酵产品的需求急剧增加。我国核苷类发酵行业亟需创建自有知识产权高性能工业菌种,提高我国核苷产业的国际竞争力。
温廷益研究组前期与已有文献均采用传统的“进、通、节、堵、出”代谢工程方法从头构建核苷工程菌,但存在产量低、生长缓慢等缺点,难以进行菌种的进一步改造与优化(Biotechnol Lett, 2011, 33:1575-1580.)。
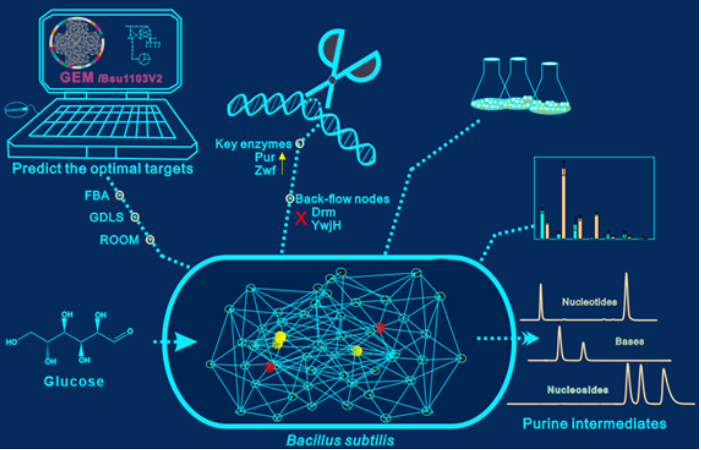
在此基础上,研究组继续以模式菌枯草芽胞杆菌W168为研究对象,利用基因组代谢网络模型对嘌呤核苷代谢流量和生物量进行分析,运用局部搜索启发式算法(GDLS)和最小开关调整算法(ROOM)预测与筛选最佳靶点。发现了两个关键回流节点Drm(PPP-嘌呤核苷途径)和YwjH(PPP-EMP)能有效解除生物量和嘌呤核苷合成之间的竞争关系。通过改造回流节点Drm,嘌呤核苷降解受到了抑制,肌苷工程菌的摇瓶产量达到13.98-14.47g/L,提高了20倍以上,且细胞生长无明显抑制。进一步解除嘌呤操纵子反馈抑制,嘌呤核苷的合成也得到了明显增强。将回流节点YwjH和Zwf相结合,提高了核苷载流途径PPP的代谢流量,肌苷产量提高到了22.01±1.18g/L。在此基础上,首次获得了能够合成肌苷、腺苷和鸟苷等嘌呤核苷通用底盘细菌,并建立了代谢开关调控的发酵过程。目前,肌苷工程菌的摇瓶产量达到25.81±1.23g/L,是文献报道的从头构建工程菌的最高产量。相关菌种已授权和受理专利各一件(ZL201510977763.6, 202110841732.3),获得了自主知识产权的肌苷工程菌种。
研究组在计算机指导下从细胞整体水平上分析嘌呤核苷合成的代谢调控机理,预测与筛选有效靶点。通过最优的改造策略快速获得了高效合成肌苷的工程菌以及通用底盘菌,为肌苷、鸟苷等核苷生产菌的选育提供了新的改造策略和实践经验。
上述研究结果近期发表于Biotechnology for Biofuels and Bioproducts期刊(原刊物名为Biotechnology for Biofuels),题为“In silico-guided metabolic engineering of Bacillus subtilis for efficient biosynthesis of purine nucleosides by blocking the key backflow nodes”,邓爱华副研究员为第一作者,温廷益研究员为通讯作者。
以上研究得到了中国科学院战略性先导专项A(鸿鹄专项,XDA17010503)、国家自然科学基金面上项目(31570083和31170103)和中国科学院绿色过程制造创新研究院(IAGM-2019-A02)的资助。